摘要
本文主要探讨了非甾抗炎药的合成和抗炎镇痛活性。非甾体抗炎药(NSAIDs)是一种不需要甾体构成的解热镇痛抗炎药。非甾体抗炎药自阿司匹林于1898年首次合成后,100多年来已有上千个品牌上市,这类药品还有阿司匹林、对乙酰氨基酚等,在临床治疗上普遍用作骨关节炎、类风湿性关节炎、各类发热和各类酸痛病症的舒缓。非甾抗炎药的合成方法有很多,药物合成的效果也不一样,我们要择优选择更合适的方法,以便大规模的制备。我们经过用动物实验来评估合成的NSAIDs的抗炎镇痛活性,对其进行活性分析,对临床工作提供理论支持。结论本研究中合成的非甾类抗炎药有优异的抗炎和镇痛效果。
关键词:非甾体抗炎药;抗炎;镇痛;活性分析
一、绪论
(一)非甾类抗炎药药用机理
非甾类抗炎药(NSAIDs)是一种临床上广泛应用的药物,其药理作用广泛,具有高效的镇痛作用和抗炎作用[1]。这类药物的作用机制是通过抑制特定部位PGs类物质的生成,从而达到抑制炎症反应的目的[2]。该类物质的不良反应也与此机制有关,PGs类物质还有保护胃肠道的功能,抑制该类PGs的合成就会使胃肠道失去保护,进而产生溃疡和胃出血等不良反应[3]。因此非甾体抗炎药物在临床诊断过程中也得到了大量应用。虽然非甾体抗炎药物存在着多种不同制备方法,但该药的主要效应功能机制仍有着高度统一性,关键在于控制了单环氧化酶的生人工物全合成。因为前列腺素会提高机体的严重疼痛程度,而单环氧化酶则可以控制前列腺素转变。由此可见,非甾体抗炎药物有着非常重要的抗炎止痛功用。
(二)计算机药物合成的重要性
随着现代科技的发展和工艺技术的改善,人们对药物的制备的设计也有了新的发展方向。计算机辅助医药设计是一项日益蓬勃发展的新兴学科,在近年来受到了人们的广泛关注,,因为它的存在可以极大的提高的药品的设计开发的速度,同时也可以对非甾类抗炎药的生物合成设计工作起关键作用。
(三)非甾类抗炎药合成的方向
相交较于以前的药物合成工艺,现在的生物合成朝绿色、环境污染较小的的工艺发展。该文中也采用了一种非甾类抗炎药(阿司匹林)的设计合成方法,并分析了多种合成方法的优缺点。还采用了阿司匹林的二种制备实验方法,来检验制备过程中的优缺点,从而确定了今后的同一非甾体抗炎药也要坚持绿色合成设计,以尽量减少对自然环境和人类健康的损害。
(四)非甾类抗炎药抗炎镇痛活性的确定
经过大量的研究文献和文献,来证明非甾体抗炎药有着更广抗炎止痛作用,在治疗中有着广泛的应用;通过动物实验(扭体法和热板法)来了解非甾体抗炎药的抗炎、镇痛活性。
二、目标物的合成
(一)计算机和新技术的应用
在计算机技术尚未广泛应用以前,人类已经经过大规模的药品制备试验,并筛选了许多药品,但是这些方法效果很慢,成绩也不明显。但近些年由于计算机科学的发展,软体和硬件都得到了极大的改善,进而为药品的制备有了全新的方法。计算机辅助药物设计是目前最主要的新药合成方法,它是指运用仿真新药和受体生物大分子间的作用,并运用分析结果与已有药物分子与生物活性物质之间关系,合理地选择新结构以及先导物质的新药研究设计方法。通过计算机模拟结构设计药物,高通量筛选,极大地降低了药物合成的成本和时间[4]。通过对疾病机制的掌握,针对特定受体和蛋白,合理设计药物,效率更高。并且能够通过计算机对设计完成的药物进行再优化,这点是传统药物设计无法比拟的[5]。
随着理论计算技术、X射线晶体学、核磁共振技术和结构与生物测量等现代科学技术的逐渐成熟,已可以得到研制对象的三维分子信息,同时由于计算机视觉的发达也可以对药物制备流程进行设计,通过计算机控制药物的分子,以便准备生产需要的物质。目前应用较为广泛的技术是分子对接技术,该技术利用配体-受体结合原理对药物分子构型进行研究,通过模拟药物与受体之间是否能够有效结合来调整化合物的结构,即在酶或者受体的结构下,设计与之相搭配的化合物,并且模拟结合模式,计算出药物的结合效率[6]。由于配体与接受器之间的关系它们相互影响、结构更加复杂。配体在不同的药剂中,其分子结构可以改变,还需考虑热力学过程方可对药剂准确设计。
(二)非甾体抗炎药物的合成方法
目前非甾体抗炎药物仍是在国内使用范围较大的药品种类之一,这类有阿司匹林、对乙酰氨基酚、双氯芬酸、布洛芬等,该类药品通常兼具抗炎、镇痛等功效。有关于市面上的药品方面,我选择了常规的阿司匹林生产方法,而阿司匹林的生产又经过多年的发展,已经出现了多种方式,就在其制备方面,我们提出以草酸根、维生素c、等物质作为了生产阿司匹林的最佳催化剂,而这种方式不但均绿色、方便、实用的优势外,更获得了所具备的生产纯度好、生产率快、腐蚀性小等优点,,在以下将分别说明:
1.浓硫酸催化合成阿司匹林。常规上阿司匹林都是用醋酸酐和水杨酸作为原材料,再用浓硫酸作反应催化剂,然后再经过酰化反应方式生产,但当这种方法存在时由于产能不足,原材料并没有得到至充分利用;易生成各种副反应,而且产品纯度也达不到相应要求;机械设备的热腐蚀现象十分明显,且后期使用情况复杂多变;粗产品在风干后,部分产品被强烈氧化物,且成色不佳,并有浓硫酸促进阿司匹林水解生成水杨酸等许多明显的技术问题。于是,为了解决此法对自然环境的巨大环境污染以及对生产原料的巨大损耗等各种困难,各类环保条件良好,且经济效益合理的新型生产方式逐渐受到了科学家和产业界的高度重视,并成为了各方公司竞相追求的重点开发对象。
2.无机酸催化合成阿司匹林。张武[7]和肖新荣[8]等分别考察了用三氯稀土(如LaC1、NdC1、YC1,等)和一水合硫酸氢钠作催化剂催化合成阿司匹林的反应效果。复杂化学反应的最佳配比条件大致相同:用了二十g左右的水杨酸、40g左右的醋酸酐、以及相应的催化物,在八十℃条件下化学反应三十min,结果产品的总收率依次超过了九十五型%和百分之八十六点四,取得了非常完美的实验效果,在复杂化学反应条件基本恒定的情况下,与催化物质相互作用,产品数基本保持恒定。所以本法既有产品分解过程简单,与催化合成物质可进行或重复的优点,又可以节约资源。三氯稀土是一个简便易得的Lewis酸,对机械设备的腐蚀性相应较少、无污染、可溶性强且对循环再生使用也十分简便,所以有着非常广泛的应用前景,是一个对自然环境良好的催化合成产品。可期成为有效减少由传统浓酸所产生的环境污染问题,从而满足目前绿色化工技术发展所要求的标准,但其较为昂贵的售价也在很大程度上限制了它更广泛的应用前景。
3.草酸催化合成阿司匹林。草酸是较一般的二元有机酸,具备较高的酸性,但相对无机酸其酸性则弱得多。隆金桥[9]等以草酸为催化剂来探究其催化合成阿司匹林的效果,并讨论了原料物质的量之比、催化剂用量、反应时间、反应温度对产品收率的影响。结果:当酸酐产物的重量之比为1:3,草酸剂量大约为零点五克,化学反应时间为五十分钟内,化学反应温度大约为八十℃,与阿司匹林收比可达百分之九十一点五,因此产品纯度较高。故本工艺具备节约资源、对仪表装置的污染较小、操作简便、催化剂用量小、产物易于提纯等优势,且应用范围广,效益发展潜力极大。
4.碳酸钠催化合成阿司匹林。钟国清[10]以无水碳酸钠为催化剂,用微波合成法对阿司匹林的合成进行了尝试,阿司匹林粗产品收率最高可达95.4%.而且本法与一些常见的加热方式相比,反应、产物收率以及提纯条件均有了很大程度的改善,对周围环境也基本完全没有了环境污染。但当然它也具有缺陷,表现在:控制参数复杂不便于掌握、要求的微波方式技术功耗过大,使得很难获得符合要求的反应时间过长,导致温度控制较复杂、在反应过程中会使系统的油温过高,引起生成了大量黄色油状物、从而导致对最终产品的分离与提纯困难度较大,相比之前收率也将大大降低。尽管微波辐照的制备反应速度比另外许多方式都要快得多,但在向产业化规模转变的流程中仍面临着不少问题,还值得继续深入研究和探讨。此外草酸钠、固态的氢氧化钠水溶液等,都是生产阿司匹林的良好碱性催化物质。在应用其催化生产阿司匹林的流程中,也分别取得了很好的效应。
5.维生素C催化合成阿司匹林。维生素C也是很普遍的维生素类药物,因为价格便宜而又很易于获得,在很多以其作催化的化学反应中产生了非常好的效应。以维生素c的催化作用制备了阿司匹林,产物经提纯后的收率可以超过百分之八十四点九,从而达到了较好的实验效果。以维生素c用作催化,不但使化学反应速度比一般的催化快了数十倍,产品质量和纯化率都很高,而且同时降低了原来浓硫酸对仪表和设备的磨损和强腐蚀,对环境的污染也基本上可归零,同时还能够应用到化工制造的很多环节上,在将来势必造成了一阵热潮。
(三)浓硫酸为作为催化剂合成阿司匹林(实验)
1.化学反应化学式。本次合成用水杨酸的酚羟基与乙酐为乙酰化试剂,在以强酸或硫酸的催化效果下,由乙酐的乙酰和水杨酸的酚羟基产生酰化效应形成酯。反应如下:
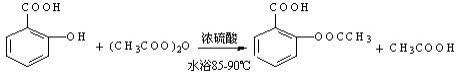
2.主要仪器及试剂。试剂:本次合成用水杨酸的酚羟基和乙酐为乙酰化试剂,在以强酸为硫酸为催化效果下,乙酐为乙酰与水杨酸的酚羟基产生酰化效应生成酯;
仪器:150mL锥形瓶,5mL吸量管(干燥,附洗耳球),100mL、250mL、500mL烧杯各一只,加热器,橡胶塞,温度计,玻璃棒,布氏漏斗,表面皿,50mL量筒,烘箱;
3.实验步骤。(1)称取1.98g水杨酸,置入锥形瓶中;在通风的环境下,用吸量管吸取3mL置于锥形瓶中,再取5滴浓硫酸(浓度V<0.2mL)置入锥型(注乙酰水杨酸溶解126℃-135℃,水杨酸与乙酐混匀后不能尽快加硫酸并升温,会产生较多副反应)。把带有玻璃管的胶塞固定在锥形瓶口,摇晃锥形瓶,使固体充分溶解。在事先预热的水浴中加温约10-15min水浴设备:用500mL的烧碗加100mL清水、沸石,用温度计调节至85℃-90℃。
(2)拔出强烈的搅拌(搅动要强烈,否则锥形瓶,将液态移动至250mL烧杯并冻结至室温(或许会没有晶析出)。加入50mL清水,进行后会分解块状物严重影响后期试验),冰水中冻结10min,结晶全部。
(3)抽滤,冷水冲洗几遍,并尽量抽干,将固体转移至表面皿,风干。
4.实验总结。(1)催化剂浓硫酸,对环境、设备、人员有危害。(2)仪器要全部干燥,药品也要实现经干燥处理,工艺设备要求高。(3)实验对于试剂的加入顺序有严格要求,证明工艺复杂。(4)在实验中对温度要求特别高(85-90℃),如果温控升高,会有水杨水杨酰酸、乙酰水杨酰水杨酸、乙酰水杨酸酐等副反应产品产生,不利于提纯,证明工艺参数严格。
综上所述,可以看出,用浓硫酸作催化剂反应后所得的阿司匹林,具有许多缺点,设备容易腐蚀、环境容易污染、作业人员不安全的特点。
(四)维生素C作为催化剂合成阿司匹林(实验)
相交老的制备方式,但近些年发展了一种较绿色制备阿司匹林的方式,是以维生素C为催化剂制备阿司匹林。维生素C(VitaminC,AscorbicAcid,抗坏血酸)为单一内酯,对生化药物有着普遍的反应特性,是一种很常用的药物、易得且无毒,在许多生物化学合成中,都发挥着良好的效果。李建伟等以维生素C催化剂制备了阿司匹林,经纯化后产率为百分之八十四点九。证明以维生素作为催化剂获得的阿司匹林产量较高,而且安全性、绿色的特点,一定会有更大前途.
1.化学返佣反应化学式。

2.主要仪器剂试剂。实验试剂:水杨酸、醋酸酐、维生素C(催化剂)
仪器:三颈瓶、人体温测定仪、恒温磁力搅拌器、布氏漏斗、锥型杯
3.实验步骤。(1)把4.0g水杨酸、醋酸酐8.5ml、大量维生素C催化剂放在三颈瓶中,置入相应的水中加热,并直入温度计,连接好实验设备后,启动加热器,开始化学实验,同时开始计时,在反应小时后,将反应容器取出,冷却到室温。在冷却过程中,阿司匹林逐渐析出,大部分固态析出后,在加50mL水溶液,放在冰水中制冷,还会有阿司匹林析出,大部分固态析出后,用布氏漏斗开始抽滤,将所得的大部分固态溶剂用冰水冲洗数次,并尽量绷紧或吸干,从而获得的阿司匹林粗品。
(2)将粗品阿司匹林重新植入干净的锥型杯中,再置入4ml95%乙醇在热水浴加热,片刻后,粗品溶解,如未完全溶解,再加少量95%乙醇,使之全部溶解,趁热过筛。
(3)把过筛的溶液加入9mL的热工水,冷冻后阿司匹林重新结晶。
(4)阿司匹林减压后过筛,吸干.经红外灯晾干后得洁白片状结晶.称品质,计生产.
4.实验总结。(1)催化剂稳定,没有危害。(2)仪器药品没有特殊要求,证实对设备要求不高。(3)工艺简单,不复杂。(4)产率高。
综述所述:使用维生素C现场没有刺激性气味,没有对设备产生腐蚀,产量高,易于制备。
三、非甾体抗炎药物抗炎镇痛活性分析
(一)动物实验镇痛分析(扭体法)
1.扭体法实验材料。药品:阿司匹林、生理盐水、醋酸、蒸馏水;
动物:小鼠(20只),雌雄各10只;
仪器:研磨体、灌胃器械
2.实验步骤。实验:小鼠雌雄各半,称重,随机分成2组,各组用苦味酸标记,分别灌胃给药:生理盐水(0.3ml),阿司匹林水溶液(11.0mg/ml,0.3ml/只)。给药30分钟后,每组小鼠腹腔注射0.68%醋酸溶液0.2ml/只,记录20分钟内小鼠扭体的反应次数。
3.对比图。结果见表3-1,数据采用均数+标准差表示,统计处理结果用两组间t检验。
表3-1
| 编号 | 对照组 | 阿司匹林 |
| 1 | 29 | 24 |
| 2 | 31 | 12 |
| 3 | 27 | 9 |
| 4 | 47 | 30 |
| 5 | 33 | 36 |
| 6 | 42 | 25 |
| 7 | 35 | 7 |
| 8 | 21 | 34 |
| 9 | 27 | 22 |
| 10 | 38 | 11 |
| 均数+标准差 | 33+7.76 | 21+10.66 |
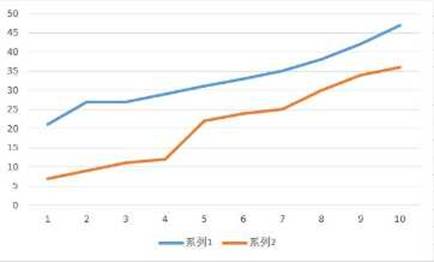
图3-1阿司匹林和对照品镇痛作用比较(红色阿司匹林组、蓝色对照组)
4.实验结果。验结果也证实,当按照人的药量换算为小鼠的药量时,给药组和对照组对比,扭体次数大大减少,证明阿司匹林起到了阵痛的作用。
(二)动物实验镇痛分析(热板法)
1.实验材料。药品:阿司匹林溶液40mg/ml、生理盐水;
动物:昆明雌性小鼠15只
仪器:热板、灌胃针、注射器
2.实验步骤。给药前通反应时间的测定:热板温度55+0.5℃,小老鼠放置在热板上,并立即计时至痛舔后足次数;给药(共计3组,每组5只):一组小老鼠不给得(对照组),另两组分别给生理盐水和阿司匹林;给药后15、30min分别测舔后足次数。
3.对比图。
表3-2
| 时间 | 对照组 | 生理盐水 | 阿司匹林 |
| 15 min | 24.68+12.9 | 21.75+15.26 | 23.81+19.66 |
| 30 min | 29.52+19.42 | 16.54+9.85 | 14.9+2.77 |
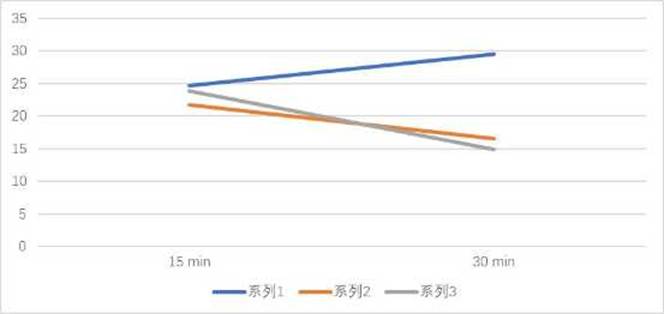
图3-2(系列1对照组、系列2生理盐水、系列3)
3.实验结果。给药阿司匹林能起到正统的作用。
(三)动物实验抗炎分析
1.实验材料。药品:0.93%阿司匹林、生理盐水
动物:小鼠(20只)
仪器:足趾体积测试器械、灌胃器械2个、注射器2个
2.实验步骤。小鼠20只,分为2组:对照组(生理盐水)、阿司匹林组,用灌胃器械分组给药,用未稀释蛋清0.05ml分别注射(对照组、组)小鼠两后肢足趾中部。在不同时间段用足趾体积测试器械测量小鼠后足的体积,计算各组小鼠后足体积增加百分率,最后分别绘制2个组的时效曲线。
本站文章通过互联网转载或者由本站编辑人员搜集整理发布,如有侵权,请联系本站删除。
